Class 10 Science Chapter 1 रासायनिक अभिक्रियाएँ और समीकरण
Class 10 Science Chapter 1 रासायनिक
अभिक्रियाएँ और समीकरण
एनसीईआरटी सोलूशन्स क्लास 10 विज्ञान अध्याय 1
एनसीईआरटी सोलूशन्स क्लास 10 विज्ञान अध्याय 1 पाठ्य पुस्तक में प्रश्न
प्रश्न 1.
हवा में जलाने से पहले मैग्नीशियम रिबन को क्यों साफ करना चाहिए?
उत्तर:
मैगनीशियम रिबन की सतह पर साधारणतया बेसिक मैग्नीशियम कार्बोनेट का लेप होता है। यह मैग्नीशियम हाइड्रॉक्साइड और मैग्नीशियम कार्बोनेट का मिश्रण है और नम हवा की क्रिया से धातु की सतह पर धीरे-धीरे जमा हो जाता है। धातु के संपर्क में आने पर कोटिंग या परत धातु को जलने से रोकती है। मैग्नीशियम ऑक्साइड की परत को हटाने के लिए रिबन को हवा में जलाने से पहले सतह को अच्छी तरह से रेत के कागज से साफ किया जाना चाहिए।
प्रश्न 2.
निम्नलिखित रासायनिक अभिक्रियाओं के लिए संतुलित समीकरण लिखिए:
(i) हाइड्रोजन + क्लोरीन ——> हाइड्रोजन क्लोराइड
(ii) सोडियम + पानी ——> सोडियम हाइड्रोक्साइड + हाइड्रोजन
(iii) बेरियम क्लोराइड + एल्युमिनियम सल्फेट ——— > बेरियम सल्फेट + एल्युमिनियम क्लोराइड।
उत्तर:
संतुलित समीकरण प्रतीक समीकरणों के लिए लिखे जाते हैं न कि शब्द समीकरणों के लिए।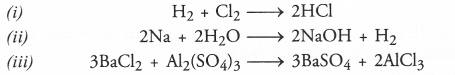
प्रश्न 3.
निम्नलिखित अभिक्रियाओं के लिए अवस्था चिन्हों के साथ संतुलित समीकरण लिखिए :
(i) पानी में बेरियम क्लोराइड और सोडियम सल्फेट के विलयन अभिक्रिया करके अघुलनशील बेरियम सल्फेट और सोडियम क्लोराइड का विलयन देते हैं।
(ii) सोडियम हाइड्रोक्साइड घोल (पानी में) हाइड्रोक्लोरिक एसिड घोल (पानी में) के साथ सोडियम क्लोराइड (पानी में) और पानी का उत्पादन करने के लिए प्रतिक्रिया करता है।
उत्तर:
प्रतिक्रियाओं के लिए संतुलित रूप में प्रतीक समीकरण हैं: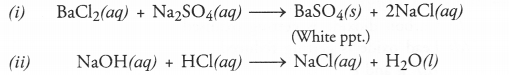
प्रश्न 4.
'X' पदार्थ के विलयन का प्रयोग सफेदी के लिए किया जाता है।
(i) पदार्थ 'X' का नाम लिखिए और उसका सूत्र लिखिए।
(ii) पदार्थ 'X' की जल के साथ अभिक्रिया लिखिए।
उत्तर:
(i) पदार्थ lX' कैल्शियम ऑक्साइड है (जिसे क्विक लाइम भी कहा जाता है)। इसका सूत्र CaO . है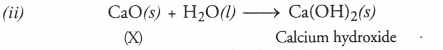
प्रश्न 5.
एक प्रयोग की सहायता से दिखाइए कि अम्लीय जल के विद्युत अपघटन में एक गैस का आयतन दूसरी गैस के आयतन का दोगुना होता है। गैस का नाम बताइए।
उत्तर:
गैस हाइड्रोजन है और इसका आयतन ऑक्सीजन से दोगुना है![]()
प्रश्न 6.
जब आप लेड (II) नाइट्रेट और पोटेशियम आयोडाइड के विलयन को मिलाते हैं,
(i) अवक्षेप का रंग कैसा होता है? शामिल यौगिक का नाम बताइए।
(ii) प्रतिक्रिया के लिए एक संतुलित रासायनिक समीकरण लिखें
(iii) क्या यह एक दोहरा विस्थापन प्रतिक्रिया है?
उत्तर:
(i) अवक्षेप का रंग पीला होता है। यौगिक सीसा (II) आयोडाइड है जिसका रासायनिक सूत्र Pbl 2 है ।
(ii) pb(NO 3 ) 2 (aq) + 2KI (aq) ———-> Pbl 2 (s) + 2KNO 3 (aq)
(iii) हां, यह दोहरी विस्थापन अभिक्रिया है।
प्रश्न 7.
कॉपर सल्फेट का रंग लोहे की कील में डुबाने पर क्यों बदल जाता है ?
उत्तर:
लोहे की कील पर कॉपर सल्फेट के विलयन से कॉपर को विस्थापित करने वाली विस्थापन अभिक्रिया के परिणामस्वरूप लोहे की कील पर कॉपर की भूरी कोटिंग हो जाती है। घोल हल्का हरा हो जाता है।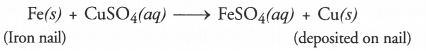
प्रश्न 8.
द्विविस्थापन अभिक्रिया का एक उदाहरण दीजिए।
जवाब:![]()
प्रश्न 9.
निम्नलिखित अभिक्रियाओं में ऑक्सीकृत होने वाले पदार्थों तथा अपचयित पदार्थों की पहचान कीजिए :![]()
उत्तर:
(i) इस अभिक्रिया में सोडियम (Na) ऑक्सीकृत होकर सोडियम ऑक्साइड (Na 2O) में परिवर्तित हो जाता है । इसका मतलब है कि ऑक्सीजन (O 2 ) कम हो गई है।
(ii) इस अभिक्रिया में हाइड्रोजन (H2) पानी (H2O) में ऑक्सीकृत हो जाता है जबकि कॉपर ( II ) ऑक्साइड (CuO) कॉपर (Cu) में अपचित हो जाता है ।
Question 10.
मैग्नीशियम रिबन हवा (या ऑक्सीजन) में एक चमकदार लौ के साथ जलता है और सफेद पदार्थ मैग्नीशियम ऑक्साइड में बदल जाता है। क्या इस प्रतिक्रिया में मैग्नीशियम का ऑक्सीकरण या अपचय हो रहा है?
उत्तर:
प्रतिक्रिया के लिए संतुलित रासायनिक समीकरण है: इस प्रतिक्रिया में![]()
मैग्नीशियम (Mg) को मैग्नीशियम ऑक्साइड (MgO) में ऑक्सीकृत किया जाता है।
एनसीईआरटी समाधान कक्षा 10 विज्ञान अध्याय 1 एनसीईआरटी अंत अभ्यास
प्रश्न 1.
नीचे दी गई प्रतिक्रिया के बारे में निम्नलिखित कथनों में से कौन सा कथन गलत है?![]()
(ए) सीसा कम हो रहा है
(बी) कार्बन डाइऑक्साइड ऑक्सीकरण हो रहा है
(सी) कार्बन ऑक्सीकरण हो रहा है
(डी) लेड ऑक्साइड कम हो रहा है
(i) ए और बी
(ii) ए और सी
(iii) ए, बी और सी
(iv) सभी गलत हैं
उत्तर:
(i) a और b दोनों गलत हैं
Pb पश्च अभिक्रिया में PbO में ऑक्सीकृत हो रहा है।
पश्च अभिक्रिया में CO , अपचित होकर C हो जाता है।![]()
प्रश्न 2.
उपरोक्त अभिक्रिया किसका उदाहरण है :
(a) संयोजन अभिक्रिया
(b) द्विविस्थापन अभिक्रिया
(c) अपघटन अभिक्रिया
(d) विस्थापन अभिक्रिया
उत्तर:
(d)। यह विस्थापन अभिक्रिया का उदाहरण है। जब जलीय घोल में अभिक्रिया की जाती है तो एल्युमिनियम (Al) धातु ने Fe 2 O 3 से लोहे (Fe) को विस्थापित कर दियाकृपया ध्यान दें कि अल प्रतिक्रियाशीलता श्रृंखला में Fe के ऊपर स्थित है।
प्रश्न 3.
क्या होता है जब तनु हाइड्रोक्लोरिक अम्ल को लोहे के भरावन में मिलाया जाता है? सही उत्तर पर निशान लगाएं:
(ए) हाइड्रोजन गैस और आयरन क्लोराइड का उत्पादन होता है
(बी) क्लोरीन गैस और आयरन हाइड्रॉक्साइड का उत्पादन होता है
(सी) कोई प्रतिक्रिया नहीं होती है
(डी) लौह नमक और पानी का उत्पादन होता है।
उत्तर:
(ए)। प्रतिक्रिया के अनुसार आयरन क्लोराइड और हाइड्रोजन गैस का उत्पादन होता है![]()
प्रश्न 4.
संतुलित रासायनिक समीकरण क्या है ? रासायनिक समीकरणों को संतुलित क्यों किया जाना चाहिए? (सीबीएसई 2013)
उत्तर:
संतुलित रासायनिक समीकरण। एक रासायनिक समीकरण को संतुलित कहा जाता है यदि:
- समीकरण के दोनों ओर विभिन्न तत्वों के परमाणु बराबर होते हैं।
- समीकरण आणविक यानी है। समीकरण में शामिल होने पर गैसें आणविक रूप में होनी चाहिए (जैसे, H 2 , O 2 , N 2 , Cl 2 आदि)
रासायनिक समीकरणों को संतुलित करने की आवश्यकता। द्रव्यमान के संरक्षण के नियम की आवश्यकता को पूरा करने के लिए रासायनिक समीकरणों को संतुलित करना पड़ता है। कानून के अनुसार,
एक रासायनिक प्रतिक्रिया में, अभिकारकों का द्रव्यमान उत्पादों के द्रव्यमान के समान होना चाहिए और यह तभी संभव है जब अभिकारकों और उत्पादों के विभिन्न तत्वों के परमाणु समान हों।
प्रश्न 5.
निम्नलिखित को रासायनिक समीकरणों में स्थानांतरित करें और उन्हें संतुलित करें:
(ए) हाइड्रोजन गैस नाइट्रोजन के साथ मिलकर अमोनिया बनाती है।
(b) हाइड्रोजन सल्फाइड गैस हवा में जलकर जल और सल्फर डाइऑक्साइड देती है।
(c) बेरियम क्लोराइड एल्युमिनियम सल्फेट के साथ अभिक्रिया करके एल्युमिनियम क्लोराइड और बेरियम सल्फेट का अवक्षेप देता है।
(d) पोटैशियम धातु जल के साथ अभिक्रिया करके पोटैशियम हाइड्रॉक्साइड तथा हाइड्रोजन गैस देती है।
उत्तर:
(ए) प्रतिक्रिया के लिए प्रतीक समीकरण है:
एच 2 + एन 2 ———> एनएच 3
समीकरण का संतुलन निम्नलिखित चरणों में किया जाता है:
चरण I: आइए हम समीकरण के दोनों ओर अभिकारकों और उत्पादों के सभी तत्वों के परमाणुओं की संख्या गिनें।
तत्वों | अभिकारकों के परमाणुओं की संख्या (LHS) | उत्पादों के परमाणुओं की संख्या |
एच | 2 | 3 |
एन | 2 | 1 |
समीकरण पर एक सरल नज़र डालने से पता चलता है कि समीकरण के दोनों किनारों पर न तो एच की संख्या और न ही एन परमाणुओं की संख्या समान है।
चरण I: दोनों पक्षों में H परमाणुओं की संख्या को समान करने के लिए, अभिकारक पक्ष पर H 2 से पहले गुणांक 3 और उत्पाद पक्ष पर NH 3 से पहले गुणांक 2 रखें।
3H 2 + N 2 ———–> 2NH 3
चरण III: गिनने पर, समीकरण के दोनों ओर N परमाणुओं की संख्या भी समान होती है (2)। इसका मतलब है कि समीकरण संतुलित है।
(बी) प्रतिक्रिया के लिए प्रतीक समीकरण है:
एच 2 एस + ओ 2 ———> एच 2 ओ + एसओ 2
समीकरण का संतुलन निम्नलिखित चरणों में किया जाता है:
चरण I: आइए समीकरण के दोनों पक्षों के सभी तत्वों के परमाणुओं की संख्या की गणना करें।
तत्वों | अभिकारकों के परमाणुओं की संख्या (LHS) | उत्पादों के परमाणुओं की संख्या |
एच | 2 | 2 |
एस | 1 | 1 |
| हे | 2 | 3 |
समीकरण पर एक सरल नज़र डालने से पता चलता है कि एच और एस परमाणुओं की संख्या दोनों तरफ बराबर है। इसी समय, O परमाणुओं की संख्या समान नहीं होती है।
चरण II: O परमाणुओं की संख्या की बराबरी करने के लिए, अभिकारक पक्ष पर O 2 से पहले गुणांक 3 और उत्पाद पक्ष पर SO 2 से पहले गुणांक 2 रखें।
H 2 S + 3O 2 ———–> H 2 O + 2SO 2
चरण III: O परमाणु अभी भी संतुलित नहीं हैं। इसे प्राप्त करने के लिए, उत्पाद पक्ष पर एच 2 ओ से पहले गुणांक 2 डालें।
एच 2 एस + 3ओ 2 ————> 2एच 2 ओ + 2एसओ 2
चरण IV:S परमाणुओं को संतुलित करने के लिए अभिकारक पक्ष पर H 2 S से पहले गुणांक 2 रखें।
2H 2 S + 3O 2 ————> 2H 2 O + 2SO 2
निरीक्षण करने पर, समीकरण के दोनों पक्षों के सभी तत्वों के परमाणुओं की संख्या बराबर होती है। इसलिए, समीकरण संतुलित है।
(सी) प्रतिक्रिया के लिए प्रतीक समीकरण है:
BaCl 2 + Al 2 (SO 4 ) 3 ———-> A1Cl 3 + BaSO 4
समीकरण का संतुलन निम्नलिखित चरणों में किया जाता है:
चरण I: आइए संख्या गिनें समीकरण के दोनों पक्षों के सभी तत्वों के परमाणुओं की संख्या।
तत्वों | अभिकारकों के परमाणुओं की संख्या (LHS) | उत्पादों के परमाणुओं की संख्या (RHS) |
बी ० ए | 1 | 1 |
ए 1 | 2 | 1 |
क्लोरीन | 2 | 3 |
| एस | 3 | 1 |
| हे | 12 | 4 |
समीकरण पर एक सरल नज़र डालने से पता चलता है कि दोनों पक्षों पर केवल बा परमाणु समान हैं। शेष परमाणुओं को संतुलित करना है। यह निम्नानुसार किया जाता है:
चरण II: Al परमाणुओं की संख्या को समान करने के लिए, उत्पाद पक्ष पर AlCl 3 से पहले गुणांक 2 रखें।
BaCl 2 + Al 2 (SO 4 ) 3 ———-> 2AICl 3 + BaSO 4
चरण III: Cl परमाणुओं को संतुलित करने के लिए, अभिकारक पक्ष पर BaCl 2 से पहले गुणांक 3 डालें।
3BaCl 2 + Al 2 (SO 4 ) 3 ———–> 2AlCl 3 + BaSO 4
चरण IV: Ba परमाणुओं को संतुलित करने के लिए, उत्पाद पक्ष पर BaSO 4 से पहले गुणांक 3 रखें।
3BaCl 2 + Al 2 (SIO 4 ) 3 ———-> 2AlCl 3 + 3BaSO 4
चरण V: निरीक्षण करने पर, समीकरण के दोनों ओर S और O परमाणुओं की संख्या भी समान पाई जाती है। इस प्रकार, समीकरण संतुलित रूप में है।
(डी) प्रतिक्रिया के लिए प्रतीक समीकरण है:
के + एच 2 ओ ———> केओएच + एच 2
समीकरण का संतुलन निम्नलिखित चरणों में किया जाता है:
चरण I। आइए हम सभी के परमाणुओं की संख्या की गणना करें दोनों तरफ के तत्व।
तत्वों | अभिकारकों के परमाणुओं की संख्या (LHS) | उत्पादों के परमाणुओं की संख्या (RHS) |
क | 1 | 1 |
एच | 2 | 3 |
हे | 1 | 1 |
समीकरण पर एक सरल नज़र डालने से पता चलता है कि समीकरण के दोनों ओर K और O परमाणुओं की संख्या समान है। इसी समय, H परमाणुओं की संख्या समान नहीं होती है।
चरण II: H परमाणुओं की संख्या को संतुलित करने के लिए, गुणांक 2 को उत्पाद पक्ष पर KOH से पहले और 2 को प्रतिक्रियाशील पक्ष पर H 2 O से पहले रखें।
K + 2H 2 O ———> 2KOH + H 2
चरण III: उपरोक्त समीकरण में K परमाणुओं की संख्या को संतुलित करने के लिए, प्रतिक्रियाशील पक्ष पर K परमाणु से पहले गुणांक 2 रखें।
2K + 2H 2 O ———> 2KOH + H 2
चरण IV: निरीक्षण करने पर, समीकरण के दोनों ओर सभी तत्वों के परमाणुओं की संख्या समान पाई जाती है। यह संतुलित है।
प्रश्न 6.
निम्नलिखित रासायनिक समीकरणों को संतुलित करें:![]()
उत्तर:
(ए) प्रतिक्रिया के लिए दिया गया प्रतीक समीकरण है:
एचएनओ 3 + सीए (ओएच) 2 ——> सीए (एनओ 3 ) 2 + एच 2 ओ
का संतुलन समीकरण निम्नलिखित चरणों में किया जाता है:
चरण I: आइए समीकरण के दोनों पक्षों के सभी तत्वों के परमाणुओं की संख्या की गणना करें।
तत्वों | अभिकारकों के परमाणुओं की संख्या (LHS) | उत्पादों के परमाणुओं की संख्या (उत्पाद) |
एच | 3 | 2 |
हे | 5 | 7 |
| एन | 1 | 2 |
| सीए | 1 | 1 |
समीकरण पर एक सरल नज़र डालने से पता चलता है कि सीए परमाणुओं की संख्या दोनों तरफ बराबर है।
चरण II: N परमाणुओं की संख्या की बराबरी करने के लिए, अभिकारक पक्ष पर HNO 3 से पहले गुणांक 2 रखें।
2HNO 3 + Ca(OH) 2 ———-> Ca(NO 3 ) 2 + H 2 O
चरण III: H परमाणुओं की संख्या को समान करने के लिए, उत्पाद पक्ष पर H 2 O से पहले गुणांक 2 डालें।
2HNO 3 + Ca(OH) 2 ———-> Ca(NO 3 ) 2 + 2H 2 O
चरण IV: निरीक्षण करने पर समीकरण के दोनों ओर O परमाणुओं की संख्या समान होती है अर्थात 8. इसलिए समीकरण संतुलित होता है।
(बी) प्रतिक्रिया के लिए दिया गया प्रतीक समीकरण है:
NaOH + H 2 SO 4 ———-> Na 2 SO 4 + H 2 O
चरण I: आइए हम दोनों पक्षों के सभी तत्वों के परमाणुओं की संख्या की गणना करें समीकरण।
तत्वों | अभिकारकों के परमाणुओं की संख्या (LHS) | उत्पादों के परमाणुओं की संख्या (RHS) |
एच | 3 | 2 |
हे | 5 | 5 |
| ना | 1 | 2 |
| एस | 1 | 1 |
समीकरण पर एक साधारण नज़र डालने से पता चलता है कि O और S परमाणुओं की संख्या दोनों तरफ बराबर है।
चरण II: Na परमाणुओं की संख्या की बराबरी करने के लिए, अभिकारक पक्ष पर NaOH से पहले गुणांक 2 रखें।
2NaOH + H 2 SO 4 ———-> Na 2 SO 4 + H 2 O
चरण III: H परमाणुओं की संख्या को समान करने के लिए, उत्पाद पक्ष पर H 2 O से पहले गुणांक 2 रखें।
2NaOH + H 2 SO 4 ———> Na 2 SO 4 + 2H 2 O
चरण IV: निरीक्षण करने पर समीकरण के दोनों ओर O परमाणुओं की संख्या समान होती है अर्थात 6. इसलिए समीकरण संतुलित है।
(सी) प्रतिक्रिया के लिए दिया गया प्रतीक समीकरण पहले से ही संतुलित है।
NaCl + AgNO 3 ———-> AgCl + NaNO 3
निरीक्षण करने पर, समीकरण के दोनों ओर सभी तत्वों के परमाणुओं की संख्या समान पाई जाती है। यह संतुलित रूप में है।
(डी) प्रतिक्रिया के लिए दिया गया प्रतीक समीकरण है:
BaCl 2 + H 2 SO 4 ———-> BaSO 4 + HCl
चरण I: आइए समीकरण के दोनों ओर सभी तत्वों के परमाणुओं की संख्या की गणना करें।
तत्वों | अभिकारकों के परमाणुओं की संख्या (LHS) | उत्पादों के परमाणुओं की संख्या (RHS) |
बी ० ए | 1 | 1 |
एच | 2 | 1 |
हे | 4 | 4 |
एस | 1 | 1 |
| क्लोरीन | 2 | 1 |
समीकरण पर एक सरल नज़र डालने से पता चलता है कि बा, एस और ओ परमाणुओं की संख्या दोनों तरफ बराबर है।
चरण II: Cl परमाणुओं की संख्या की बराबरी करने के लिए, उत्पाद पक्ष पर HCl से पहले गुणांक 2 रखें।
BaCl 2 + H 2 SO 4 ——-> BaSO 4 + 2HCl
चरण III: निरीक्षण करने पर, समीकरण के दोनों ओर H परमाणुओं की संख्या समान होती है, अर्थात 2. इसलिए, समीकरण संतुलित है।
प्रश्न 7.
निम्नलिखित प्रतिक्रियाओं के लिए संतुलित समीकरण लिखें:
(ए) कैल्शियम हाइड्रॉक्साइड + कार्बन डाइऑक्साइड ---> कैल्शियम कार्बोनेट + पानी
(बी) लेड + कॉपर क्लोराइड ---> लेड क्लोराइड + कॉपर
(सी) बेरियम क्लोराइड + सोडियम सल्फेट ———-> बेरियम सल्फेट + सोडियम क्लोराइड
( घ) जिंक + सिल्वर नाइट्रेट ———> जिंक नाइट्रेट + सिल्वर।
उत्तर:
ये सभी समीकरण शब्द रूप में हैं जबकि संतुलित समीकरण प्रतीक रूप में लिखे गए हैं।
(ए) सीए (ओएच) 2 + सीओ 2 ———-> सीएसीओ 3 + एच 2 ओ
(बी) पीबी + CuCl 2 ———-> PbCl2 + Cu
(सी) BaCl 2 + Na 2 SO 4 ———> BaSO 4 + 2NaCl
(d) Zn + 2AgNO 3 ———–> Zn(NO 3 ) 2 + 2Ag
प्रश्न 8.
निम्नलिखित प्रतिक्रियाओं के लिए संतुलित रासायनिक समीकरण लिखें और प्रतिक्रिया के प्रकार की पहचान करें:
(ए) पोटेशियम ब्रोमाइड (एक्यू) + बेरियम आयोडाइड (एक्यू) ———> पोटेशियम आयोडाइड (एक्यू) + बेरियम ब्रोमाइड (एक्यू)
( b) जिंक कार्बोनेट (aq) ———> जिंक ऑक्साइड (aq) + कार्बन डाइऑक्साइड (aq)
(c) हाइड्रोजन (aq) + क्लोरीन (aq) ——> हाइड्रोजन क्लोराइड (aq)
(डी) मैग्नीशियम (aq) + हाइड्रोक्लोरिक एसिड (aq) ————> मैग्नीशियम क्लोराइड (aq) + हाइड्रोजन (aq)।
उत्तर:
(a) 2KBr (aq) + BaI 2 (aq) ——–> 2Kl (aq) + BaBr 2 (aq)
अभिक्रिया द्विविस्थापन अभिक्रिया कहलाती है।
(बी) जेडएनसीओ 3(s) ———-> ZnO(s) + CO2 ( g)
अभिक्रिया को अपघटन अभिक्रिया कहते हैं। (
सी) एच 2 (जी) + सीएल 2 (जी) ———–> 2 एचसीएल (जी)
प्रतिक्रिया को संयोजन प्रतिक्रिया के रूप में जाना जाता है।
(डी) एमजी (एक्यू) + 2 एचसीएल (एक्यू) ———> एमजीसीएल 2 (एक्यू) + एच 2 (जी)
प्रतिक्रिया को विस्थापन प्रतिक्रिया के रूप में जाना जाता है।
प्रश्न 9.
ऊष्माक्षेपी तथा ऊष्माशोषी अभिक्रियाओं से आप क्या समझते हैं ? उदाहरण दो।
उत्तर:
एक रासायनिक प्रतिक्रिया को ऊष्माक्षेपी कहा जाता है जिसमें एक निश्चित मात्रा में ऊष्मा ऊर्जा निकलती है। जिस पात्र में अभिक्रिया की जाती है वह गर्म हो जाता है। उदाहरण के लिए,
N 2 (g) + 3H 2 (g) ——> 2NH 3 (g) + 92 kj
CH 4 (g) + 2O 2 (g) ——> CO 2 (g) + 2H 2 O (एल) + 890 kj
NaOH (aq) + HCl (aq) ———> NaCl (aq)+ H 2 O (aq) + 57.5 kj
एक रासायनिक प्रतिक्रिया को एंडोथर्मिक कहा जाता है जिसमें एक निश्चित मात्रा में ऊष्मा ऊर्जा अवशोषित होती है। जिस पात्र में अभिक्रिया की जाती है वह ठंडा हो जाता है। उदाहरण के लिए,
N 2 (g) + O 2 (g) ———-> 2NO (g) – 180 kj
C(s) + H 2 O (aq) ———-> CO (g) + H 2 ( छ) - 130 kj
प्रश्न 10.
श्वसन को ऊष्माक्षेपी अभिक्रिया क्यों माना जाता है ? (सीबीएसई 2011)
उत्तर:
श्वसन सबसे महत्वपूर्ण जैव रासायनिक प्रतिक्रिया है जो कोशिकाओं में ऊर्जा छोड़ती है। जब हम हवा में सांस लेते हैं, तो ऑक्सीजन हमारे फेफड़ों में प्रवेश करती है। यह खुद को लाल कोशिकाओं में मौजूद हीमोग्लोबिन से बांधता है और शरीर में मौजूद लाखों कोशिकाओं तक ले जाता है। इन कोशिकाओं में श्वसन होता है और ग्लूकोज के दहन के साथ कार्बन डाइऑक्साइड पानी और ऊष्मा ऊर्जा का उत्पादन होता है।![]()
प्रश्न 11.
अपघटन अभिक्रियाओं को संयोजन अभिक्रियाओं के विपरीत क्यों कहा जाता है? इन अभिक्रियाओं के समीकरण लिखिए।
उत्तर:
संयोजन प्रतिक्रिया को उस प्रतिक्रिया के रूप में परिभाषित किया जा सकता है जिसमें दो या दो से अधिक पदार्थ उपयुक्त परिस्थितियों में मिलकर एक नया पदार्थ बनाते हैं। उदाहरण के लिए,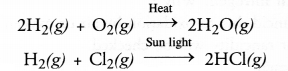
एक अपघटन प्रतिक्रिया को उस प्रतिक्रिया के रूप में परिभाषित किया जा सकता है जिसमें एक पदार्थ उपयुक्त परिस्थितियों में दो या दो से अधिक पदार्थों में विघटित या विभाजित हो जाता है।
उदाहरण के लिए,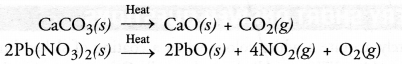
यह निष्कर्ष निकाला जा सकता है कि एक निश्चित पदार्थ संयोजन प्रतिक्रिया में बनता या संश्लेषित होता है और यह अपघटन प्रतिक्रिया में टूटता या विभाजित होता है। इसलिए, दोनों प्रतिक्रियाएं एक दूसरे का विरोध करती हैं।
प्रश्न 12.
प्रत्येक अपघटन अभिक्रिया के लिए समीकरण लिखिए, जिसमें ऊष्मा, प्रकाश और विद्युत के रूप में ऊर्जा की आपूर्ति की जाती है।
जवाब: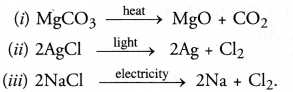
प्रश्न 13.
विस्थापन और द्विविस्थापन अभिक्रियाओं में क्या अंतर है? इन अभिक्रियाओं के समीकरण लिखिए। (सीबीएसई 2011)
उत्तर:
विस्थापन अभिक्रिया में विलयन में घुले यौगिक में एक तत्व दूसरे तत्व का स्थान लेता है। उदाहरण के लिए,
Fe(s) + CuSO 4 (aq) ——> FeSO 4 (aq) + Cu(s)
द्विविस्थापन अभिक्रिया में, दोनों अभिकारक अणुओं में से एक-एक घटक का आदान-प्रदान होकर उत्पाद बनते हैं। उदाहरण के लिए,
HCl (aq) + NaOH (aq) ———> NaCl (aq) + H 2 O (aq)
प्रश्न 14.
चांदी के शोधन में, सिल्वर नाइट्रेट के विलयन से चांदी की प्राप्ति में तांबा धातु द्वारा विस्थापन शामिल है। शामिल रासायनिक समीकरण लिखिए।
उत्तर:
विस्थापन प्रतिक्रिया के लिए रासायनिक समीकरण है:
Cu(s) + 2AgNO 3 (aq) ———-> Cu(NO 3 ) 2 (aq) + 2Ag (s)।
प्रश्न 15.
अवक्षेपण अभिक्रिया से आप क्या समझते हैं ? उदाहरण देते हुए स्पष्ट कीजिए।
उत्तर:
अवक्षेपण अभिक्रिया में, अभिक्रिया के दौरान बनने वाला उत्पाद विलयन में नहीं घुलता और पात्र (बीकर या ट्यूब) की सतह पर जम जाता है। इसे अवक्षेपण के रूप में जाना जाता है। उदाहरण के लिए,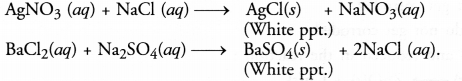
प्रश्न 16.
निम्नलिखित को ऑक्सीजन के लाभ या हानि के संदर्भ में प्रत्येक के दो उदाहरणों के साथ समझाइए,
(a) ऑक्सीकरण
(b) अपचयन।
उत्तर:
(ए) ऑक्सीकरण में किसी पदार्थ द्वारा रासायनिक प्रतिक्रिया में ऑक्सीजन का लाभ शामिल होता है। उदाहरण के लिए,
(बी) कमी में रासायनिक प्रतिक्रिया में किसी पदार्थ से ऑक्सीजन की हानि शामिल है। उदाहरण के लिए,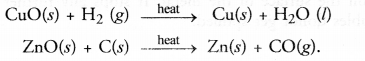
Question 17.
एक चमकदार भूरे रंग का तत्व 'X' हवा में गर्म करने पर काले रंग का हो जाता है। तत्व 'X' तथा बनने वाले काले रंग के यौगिक का नाम लिखिए। (सीबीएसई 2013)
उत्तर:
तत्व 'X' कॉपर है और काले रंग का यौगिक कॉपर (II) ऑक्साइड है जिसे कप्रिक ऑक्साइड भी कहा जाता है।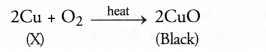
प्रश्न 18.
आप लोहे की वस्तुओं पर पेंट क्यों लगाते हैं ?
उत्तर:
पेंट लोहे की सतह पर एक सुरक्षात्मक परत बनाता है। ऑक्सीजन और नमी (हवा में मौजूद) दोनों का लौह धातु की सतह से सीधा संपर्क नहीं हो सकता है। इसलिए, सतह जंग लगने से सुरक्षित हो जाती है।
प्रश्न 19.
तेल और वसा युक्त खाद्य पदार्थों को नाइट्रोजन से प्रवाहित किया जाता है। क्यों ?
उत्तर:
तेल और वसा युक्त खाद्य पदार्थ या खाद्य पदार्थ हवा या ऑक्सीजन द्वारा ऑक्सीकरण के कारण खराब हो जाते हैं। यदि कंटेनर या बैग को नाइट्रोजन से भर दिया जाता है, तो ऑक्सीकरण या खराब होने की जाँच की जाएगी।
प्रश्न 20.
निम्नलिखित पदों को प्रत्येक के एक-एक उदाहरण द्वारा स्पष्ट कीजिए।
(ए) जंग
(बी) जंग खा रहा है।
उत्तर:
जंग को लंबे समय तक खुले में रखने पर कुछ धातुओं की सतहों को धीरे-धीरे खाने की रासायनिक प्रक्रिया के रूप में परिभाषित किया जा सकता है।
अक्सर, जब हम लंबे समय के बाद किसी कार की बोनट खोलते हैं, तो हमें बैटरी के टर्मिनलों के आसपास एक जमा राशि मिलती है। यह टर्मिनलों के क्षरण के कारण है। चांदी की सतह पर काली परत और तांबे की सतह पर हरी परत जंग के उदाहरण हैं। लोहे के मामले में, जंग को जंग कहा जाता है। जंग एक रासायनिक पदार्थ है जो नरम होने के साथ-साथ झरझरा भी होता है। यह भूरे रंग का होता है और नम हवा (सीओ 2 और एच 2 . युक्त) की रासायनिक क्रिया से बनता हैओ) लोहे पर। यह मूल रूप से एक ऑक्सीकरण प्रतिक्रिया है और जंग का सूत्र Fe 2 O 3 .xH 2 O है। यह प्रकृति में बहुत धीमा है और एक बार शुरू होने पर जारी रहता है।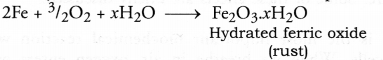
जंग और जंग दोनों ही बहुत हानिकारक होते हैं और इमारतों, रेलवे पटरियों, ऑटोमोबाइल और अन्य वस्तुओं / सामग्रियों को नुकसान पहुंचाते हैं जहां धातुओं का उपयोग किया जाता है। हम अक्सर सुनते हैं कि एक पुरानी इमारत अपने आप गिर गई है जिससे जान-माल का नुकसान हुआ है। यह लोहे में जंग लगने के कारण है जिसका उपयोग संरचनाओं को विशेष रूप से छत बनाने में किया जाता है। जंग भी संगमरमर से बनी मूर्तियों को लगातार नुकसान पहुंचाती है जो रासायनिक रूप से कैल्शियम कार्बोनेट (CaCO 3 ) है) बारिश के पानी में मौजूद सल्फ्यूरिक एसिड और नाइट्रिक एसिड दोनों कैल्शियम कार्बोनेट को घोलकर क्रमशः कैल्शियम सल्फेट और कैल्शियम नाइट्रेट बनाते हैं।
CaCO 3 + H 2 SO 4 ———— > CaSO 4 + CO 2 + H 2 O
CaCO 3 + 2HNO 3 ————> Ca(NO 3 ) 2 + CO 2 + H 2 O
इसके अलावा, वातावरण में मौजूद हाइड्रोजन सल्फाइड गैस (एच 2 एस) के निशान कैल्शियम सल्फाइड के कारण इन मूर्तियों पर काले धब्बे बन जाते हैं जो कि काले रंग का होता है।
CaCO 3 + H 2 S ———–> CaS + H 2 O + CO 2
जंग ने 'ताज महल' सहित हमारे ऐतिहासिक स्मारकों को भारी नुकसान पहुंचाया है, जिसे आठवां आश्चर्य माना जाता है। संगमरमर रासायनिक रूप से CaCO 3 है । प्रदूषित हवा में H2SO4 और HNO3 दोनों के साथ - साथ H2S गैस भी होती है। वे CaCO3 के साथ रासायनिक रूप से प्रतिक्रिया करते हैं ऊपर दिखाये अनुसार। फलस्वरूप यह ऐतिहासिक स्मारक, जो भारत का गौरव है, जीर्ण-शीर्ण हो रहा है। 'ताजमहल' और इसी तरह के अन्य स्मारकों की रक्षा के लिए हर संभव प्रयास किया जाना चाहिए जो हमारे खजाने हैं। संक्षारण (या जंग लगना) केवल धातुओं में होता है। हम धातु और अधातु पर अध्याय 3 में इसका विस्तार से अध्ययन करेंगे और क्षरण को रोकने के उपायों का अध्ययन करेंगे।